Sommaire :
La maladie de Charcot est une maladie neurodégénérative qui altère les cellules nerveuses contrôlant les mouvements. Évoluant progressivement, elle engendre rapidement une paralysie complète des membres et des muscles de la bouche et de la gorge. Aucun traitement thérapeutique n’existe à ce jour pour guérir d’une sclérose latérale amyotrophique (SLA). Une prise en charge adaptée peut toutefois améliorer l’espérance de vie des patients. Quelle est-elle ? Quels en sont les effets ? Où en est la recherche ? Voici quelques explications.
La maladie de Charcot : une pathologie difficile à diagnostiquer
La maladie de Charcot est souvent identifiée tardivement car elle peut être confondue avec d’autres maladies. Ainsi, des maladies infectieuses (maladie de Lyme, brucellose…) ou des pathologies proches de la SLA ont des signes cliniques identiques. Une tumeur comprimant la moelle épinière ou une intoxication (au plomb, à l’arsenic, à l’aluminium…) génèrent aussi des symptômes similaires.
Aucun protocole spécifique n’existe pour détecter la maladie de Charcot. Il faut donc tout d’abord vérifier qu’une autre maladie n’est pas à l’origine des troubles constatés (chutes, crampes, difficultés d’élocution…).
Évaluer le fonctionnement des muscles et des nerfs
Le neurologue réalise un électromyogramme (EMG) pour vérifier le fonctionnement des muscles et des nerfs. Un faible courant électrique est envoyé très brièvement dans les fibres du système nerveux périphérique. Ce message artificiel est transmis aux muscles. Des électrodes posées sur la peau ou une aiguille insérée dans les muscles permettent d’enregistrer la réponse à l’influx nerveux.
Si le patient est atteint d’une SLA, l’EMG montre un affaiblissement des nerfs transmettant les ordres aux muscles. Cette dénervation se situe dans les zones du corps où sont apparus les premiers symptômes (membres, cou, torse).
Vérifier l’état de la moelle épinière
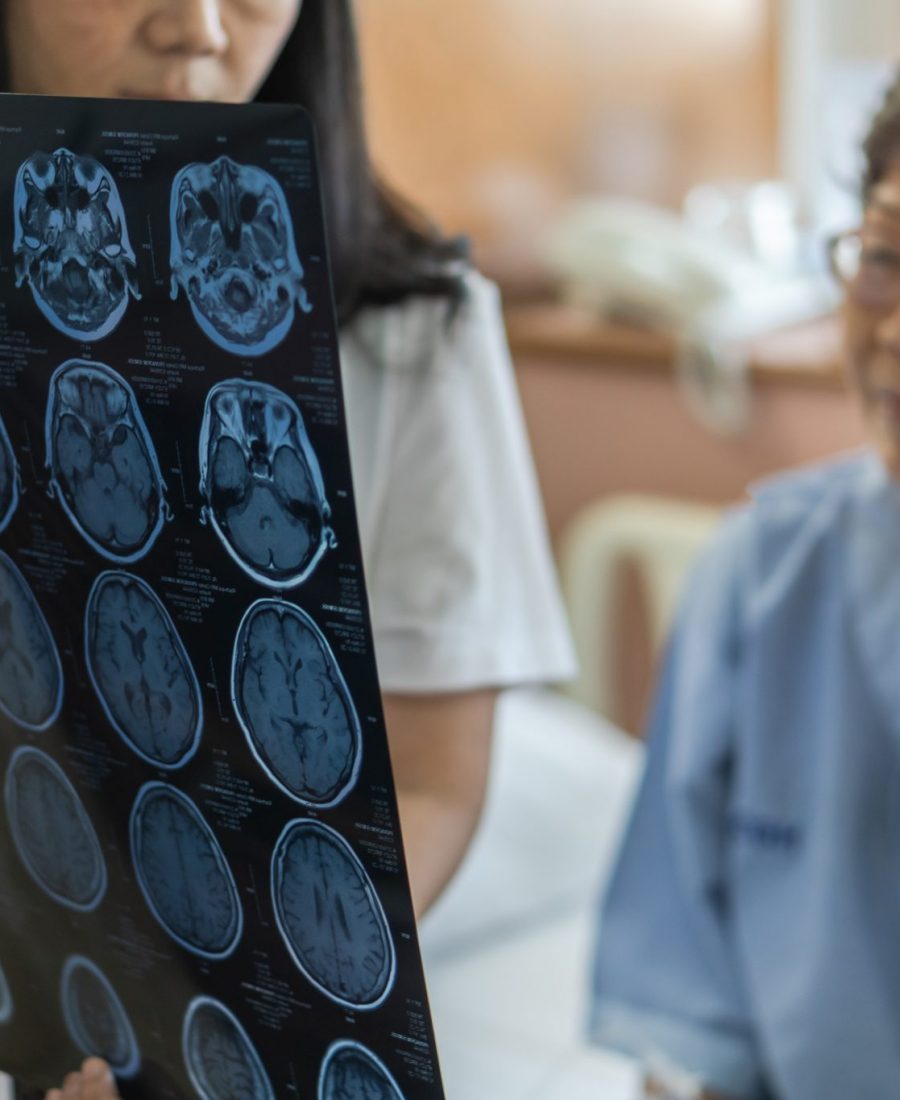
Un scanner ou une IRM (imagerie par résonance magnétique) peut être pratiqué. Ces examens permettent de repérer une blessure ou une altération de la moelle épinière ou du cerveau. Si l’image ne révèle aucune anomalie, c’est que les symptômes sont bien ceux d’une SLA.
Une ponction lombaire peut également être effectuée pour analyser le liquide céphalo-rachidien, liquide circulant autour de la moelle épinière. En cas de SLA, aucune infection n’est détectée.
Pratiquer une étude génétique
Les formes héréditaires sont peu fréquentes et ne représentent que 10 % des SLA. Les antécédents familiaux sont pris en compte si au moins deux parents directs ont été atteints par cette maladie. Il peut s’agir du père, de la mère, des frères et sœurs ou des grands-parents du patient. Une analyse génétique permet de vérifier que la mutation d’un gène n’est pas à l’origine des symptômes. Si celle-ci est avérée, le patient est atteint d’une SLA de forme familiale.
Une prise en charge à effectuer rapidement
En France, 5 000 à 7 000 personnes[1] sont atteintes de SLA et 2 300 nouveaux cas sont diagnostiqués chaque année[2].
Même si le pronostic de cette maladie est sévère, il est possible de ralentir sa progression. Une prise en charge adaptée permet, en effet, au patient de voir ses troubles et sa perte d’autonomie régresser.
Un seul traitement connu
Un seul médicament, le riluzole, dispose d’une autorisation de mise sur le marché. Il est prescrit dès qu’il y a une suspicion de SLA pour diminuer le taux de glutamate. En effet, ce neurotransmetteur excitateur du système nerveux central semblerait intervenir dans le processus d’altération des cellules nerveuses contrôlant les mouvements.
En arrêtant la libération du glutamate, ce traitement pourrait freiner la dégénérescence des cellules nerveuses et limiter l’évolution des symptômes.
D’autres médicaments peuvent être prescrits en complément pour réduire les troubles associés à la SLA (douleurs musculaires, crampes, constipation, etc.).
Des professionnels au chevet du patient
La prise en charge du malade par différents professionnels de santé peut sensiblement améliorer son confort au quotidien. Elle augmente également son espérance de vie. Ainsi, 20 % des malades bénéficiant d’un accompagnement adapté vivent plus de 5 ans et 10 % plus de 10 ans.
Entretenir la mobilité
Le kinésithérapeute et l’ostéopathe maintiennent la motricité du patient et l’aident à se détendre.
Pour renforcer l’effet de ces séances, une activité physique régulière adaptée au degré d’autonomie du malade sera bienvenue. Les activités douces (jardinage, marche, danse, natation, vélo…) sont particulièrement recommandées aux personnes souffrant de SLA.
Pouvoir communiquer et se nourrir
L’orthophoniste intervient contre les troubles affectant la parole et la déglutition. Il préserve ainsi le plus longtemps possible la capacité à communiquer et à se nourrir. Le nutritionniste donne des conseils facilitant la prise des repas malgré les difficultés à déglutir et à mastiquer. En mixant les aliments, en consommant des boissons épaissies, des produits faciles à avaler (œuf, laitage, compote, entremets…), le malade réduit le risque de fausses routes et d’étouffement. Il peut donc continuer à s’alimenter, limitant ainsi les problèmes de dénutrition et de déshydratation qui ne font qu’accentuer sa faiblesse musculaire.
Gérer la perte d’autonomie
L’ergothérapeute, quant à lui, apporte de précieux conseils pour aménager le domicile du patient afin de limiter chutes et accidents. Il montre à la personne malade comment réaliser différemment certains gestes afin de compenser sa perte d’autonomie. Il prescrit également du matériel adapté à son handicap (déambulateur, orthèse pour soutenir un membre ou une articulation, fauteuil roulant).
Favoriser l’acceptation de la maladie
La prise en charge physique de la maladie est encore plus efficace si elle est complétée par un suivi psychologique. Cet accompagnement doit être proposé au patient et à son entourage dès l’annonce du diagnostic. Il peut se poursuivre tout au long du processus d’évolution de la pathologie.
| ⊃ Bon à savoir En France, 19 centres de référence sont dotés d’une équipe pluridisciplinaire spécialisée dans la prise en charge de cette maladie. |
Où en est la recherche ?
Les causes de la maladie de Charcot restent difficiles à cerner. Toutefois, depuis quelques années, les scientifiques envisagent la SLA comme une famille générique regroupant plusieurs maladies du motoneurone.
Ainsi, constituer des groupes plus homogènes de patients faciliterait la recherche de traitements efficaces. La répartition pourrait se faire sur les causes de la maladie (mutations génétiques concernées) et sur ses manifestations (symptômes).
De même, connaître les marqueurs biologiques de la SLA permettrait d’identifier les patients susceptibles de la développer. Grâce à cette avancée, ils pourraient être pris en charge dès l’émergence des premiers signes cliniques. Une autre piste de recherche joue sur la compréhension des processus physiologiques en jeu dans la maladie de Charcot. En effet, savoir quels mécanismes entraînent la destruction des motoneurones aiderait à mettre au point de nouveaux traitements.
Par ailleurs, des études cliniques actuellement en cours testent des médicaments limitant la destruction des neurones ou favorisant leur régénération.
____________________________________________________________________________________________________________
[1] Source : Association pour la recherche sur la SLA (ARSLA)
[2] Données Santé publique France.
[3] La maladie touche d’abord les muscles des membres (bras, jambes)
[4] La SLA atteint initialement les muscles de la bouche et de la gorge.